混凝土生物破坏与海底隧道微生物群落,和应对的科技进展

文 |黛月白
编辑 | 黛月白
引言
近年来,海底隧道建设成为了现代交通发展的重要组成部分,随着时间的推移,一些海底隧道的钢筋喷射混凝土遭受了恶化现象,这引起了研究人员的关注,更加令人惊讶的是,研究发现这些恶化的混凝土内,蕴藏着各种不同的微生物群落。
混凝土生物破坏
混凝土的生物破坏,是由微生物的代谢活动引起的,包括细菌、古菌、真菌和藻类,它导致了混凝土结构和功能的不良变化,开裂、剥落、凹坑和混凝土基质中化合物的溶出,微生物需要在混凝土表面定居并形成生物膜,这个过程被称为生物污垢。
生物膜提供了多种优势,易于获取营养物质,并对极端环境和侵蚀性化合物具有抵抗力。
在混凝土表面形成的生物膜中,微生物细胞,被嵌入在自产生的胞外聚合物物质中,生物膜具有高度水化和开放的结构,其中不同微生物群落的菌落之间有空隙,形成微环境的梯度。

混凝土表面的高粗糙度、孔隙和微裂纹,为生物污垢的形成提供了有利条件,混凝土的pH值在施工后通常较高,对微生物的定居具有一定的免疫性,但当pH值降低到一定程度时,生物污垢才会形成,释放出的生物酸进一步降低了混凝土的pH值,最终溶解水泥糊浆基质。
仅靠生物酸无法完全解释混凝土的全面破坏,更多是由于持续进行的微生物相互作用的影响,降低的pH值还促进了钢筋和纤维的腐蚀,生物膜中的胞外聚合物,进一步加速了钢筋的腐蚀,其中含有负电荷,促进与金属的离子和静电结合,产生了电偶反应。

微生物的活动导致了混凝土的持续破坏,混凝土的生物破坏是一个复杂的过程,不仅涉及生物酸的作用,还包括微生物相互作用和钢筋腐蚀多个因素,海底隧道等重要建筑物,科研人员需要采取适当的防护措施,以延缓混凝土的生物破坏过程,确保结构的安全和可持续发展。

奥斯陆峡湾海底隧道的微生物群落
研究人员在挪威德罗巴克附近的奥斯陆峡湾海底隧道,进行了采样,这个隧道长7,306米,宽11.5米,最大深度为海平面以下134米,岩体主要由花岗片麻岩和伟晶岩组成,其中的节理和断层带含有黏土矿物质。
采样是在三个不同的隧道位置进行的,主隧道、泵站和奥斯陆峡湾试验场地,代表两种不同的混凝土基材。主隧道和泵站的混凝土喷涂于1999年,用作永久岩体支护。这些混凝土采用了一种快速硬化水泥,水胶比为0.42。
胶凝剂含量约为514 kg/m^3,添加了5%硅灰,并添加了钢纤维增强和减水剂。根据混凝土标准NS EN 206,这些混凝土属于耐久性等级M45和强度等级B45。硫酸铝被用作凝结促进剂。

奥斯陆峡湾试验场上的混凝土耐久性试验始于2010年3月,不久后就发现了微生物生物膜,试验场的混凝土基于CEM II/AV 42,5 R,采用不同的配比制备,生物膜采样站点位于水胶比为0.43、4%硅灰、减水剂。
钢纤维和聚丙烯纤维制成的喷涂混凝土上,同样使用硫酸铝作为凝结促进剂,这种混凝土与其他两个位置的混凝土相比,对应于M45和B45,使用飞灰水泥制成的混凝土,被认为比基于CEM I的混凝土更耐久。
在评估水泥糊剂降解和钢纤维腐蚀的风险时,使用了NS EN 206的暴露等级,在所有三个研究地点和所有混凝土配比中,所使用的等级为XC2-XC3、XS3和XA3,这些混凝土在这样的环境中,被认为是耐久的。
需要注意的是,混凝土的标准环境分类,并未考虑生物膜的影响在泵站中,水的温度为13°C,在主隧道和测试点的位置大约为8-9°C,并且在过去几年中保持相对稳定,尽管科研人员没有测量与生物膜相关的水流量,但在所有位置上的主要特征是水的渗透速度较慢。

需要注意的是,从2013年开始,泵站的水负荷在空间和容量上都持续增加,与此相比,之前的13-14年期间,生物膜主要是由较小区域中的缓慢渗透水所形成,这段文字描述了对生物膜样品和水样品,进行微生物群落分析,以及化学分析的方法。
采集的生物膜样品是厚且软的,使用金属管取得样品核心,而薄生物膜则用手术刀从混凝土上刮下,采样后,样品立即在乙醇-干冰混合物中快速冷冻,并在运输过程中放置在干冰中,并在-80°C下保存,直到进行核酸提取。
一部分生物膜样品还用于化学分析,水样品则在无菌瓶中收集,并在运输到实验室期间放置在干冰中,所有水样品在分析前均经过0.45微米的过滤,用于化学分析的生物膜样品在分析前经过均质化,并在105°C下干燥。

微波消解后,使用电感耦合等离子体质谱仪以及酸按照EPA 3051协议对选择性金属进行定量分析,生物膜的总固体和挥发性固体,分别根据APHA 1998标准方法2490 A-D进行分析,水中的氯化物、硝酸盐、铵盐和硫酸盐则根据FINAS认可的方法进行分析。
这个工作流程的目标是从生物膜样本中提取DNA,并进行PCR扩增和测序,最后进行数据分析,科研人员使用Fast DNA spin kit for soil从500mg的生物膜中提取DNA,这个试剂盒可以高效地提取DNA,并且适用于土壤样本。
科研人员使用引物515′F和806 R进行PCR扩增16S rRNA基因的V4区域,这一区域可以涵盖细菌和古菌的序列,以便进行宏基因组分析,这些引物在先前的研究中已经被验证为有效。
PCR扩增后,科研人员对产物进行纯化和归一化处理,以准备测序,科研人员使用Illumina MiSeq和MiSeq试剂盒v2进行测序,Illumina MiSeq是一种高通量测序平台,可以产生大量高质量的DNA序列数据。
测序完成后,科研人员使用USEARCH v.10进行序列处理和筛选,科研人员使用MiDAS筛选数据库对序列进行分类,这样可以将不同的序列与已知的分类进行对比,以确定它们属于哪些细菌或古菌。
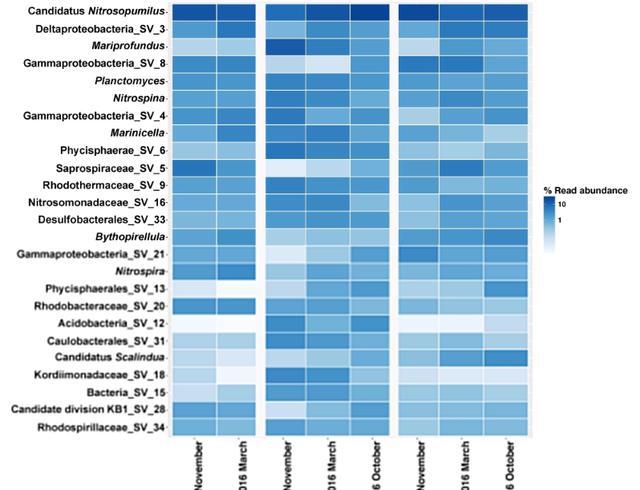
科研人员对分类的序列变异体,在这个研究中,科研人员使用了三个R包来进行多元统计学、多样性和空模型计算,以及数据可视化,科研人员使用配对Sorensen和Bray-Curtis差异,来估计样本间的β多样性,并使用主坐标分析将样本可视化。

科研人员使用置换多元方差分析,来检验样本间β多样性的差异,在vegan包中,科研人员使用标准化效应大小,来估计配对Sorensen差异,以测试样本间随机组成,科研人员使用保持物种丰富度和物种发生率的空模型,并使用quasiswap算法进行999次模拟的空模型群落。
科研人员使用picante包来计算未加权最近分类指数,并使用“taxa.labels”的空模型,进行999次迭代,以测试密切相关类群之间的系统发生聚类,为了探索微生物群落结构与生物膜,以及水的化学特性之间的关联。
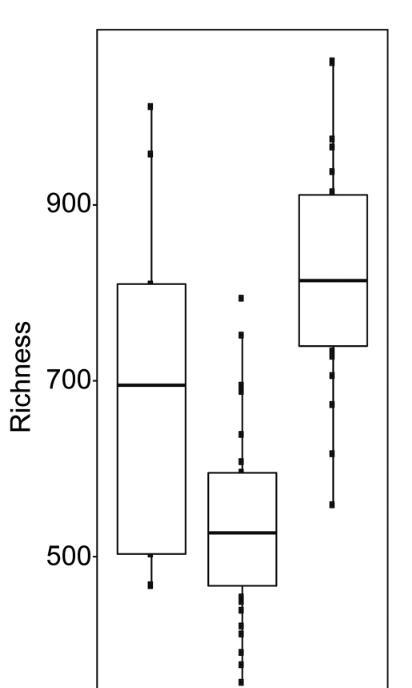
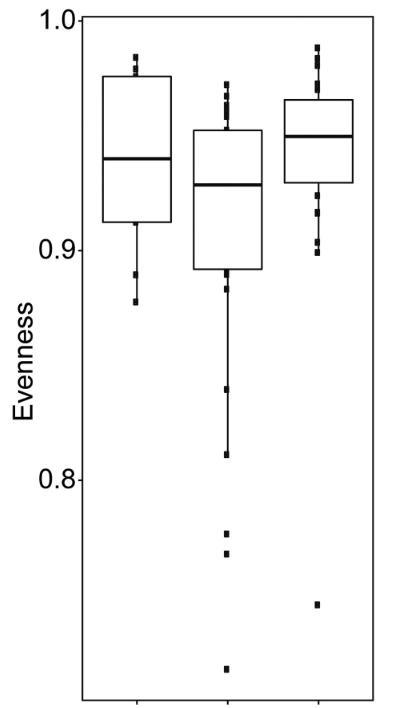
科研人员使用Welch's ANOVA,来检验群落丰富度和均匀度的差异,并使用Games-Howell检验进行事后分析,这些分析有助于科研人员理解样本间的差异和相似性,并从中推断出关于微生物群落结构及其与环境特征之间的关系。

本实验使用微传感器,对生物膜进行原位氧和pH梯度测量,氧微传感器和pH微传感器与参比电极结合使用,连接到一个多用途仪表上,并通过软件进行控制,在每次测量之前,先使用一个已使用过的微传感器估计生物膜的深度。
将微传感器尖端定位在生物膜-水界面上,并在每次测量之前等待一段时间进行微剖面测量,实验过程中,根据制造商的协议,氧传感器进行了校准,使用100%空气饱和盐水地下水在当前温度下进行校准,而pH传感器使用当前温度下的三个pH缓冲液点进行线性校准。
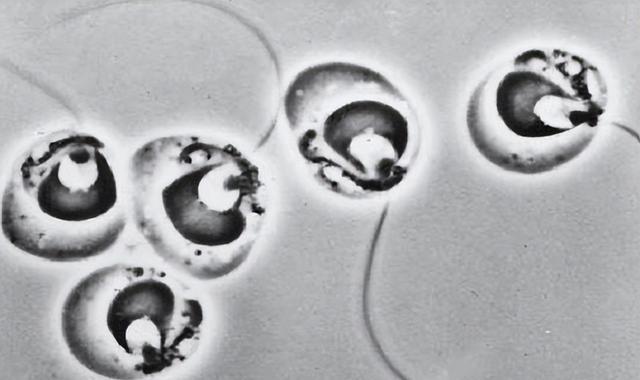
扫描电子显微镜,是一种科学仪器,用于观察微小的样品,在这个实验中,科研人员使用了一台名为Hitachi S-4800SEM的仪器,配备了能量散射X射线光谱仪,科研人员将未经涂层的手选样品固定在碳胶带上,并使用这台仪器,对样品进行了化学点分析。
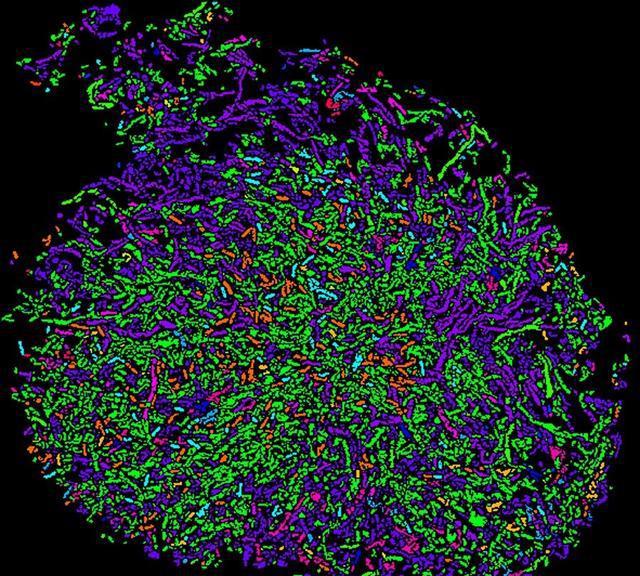
对于大多数元素,分析精度在1-2%之间,但对于碳和氮元素,精度相对较低,科研人员还捕捉了样品的反射电子图像,以提供更多的信息,科研人员使用了扫描电子显微镜和能量散射X射线光谱仪,来对未经处理的样品进行化学分析。
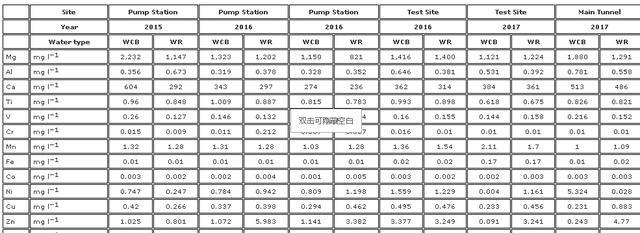
这些实验帮助科研人员了解样品的化学成分,并提供了有关样品结构和特性的详细信息,测量结果表示,奥斯陆峡湾海底隧道的盐水地下水,与海水的化学成分相似,它们的主要成分是氯化物、钠和硫酸盐,浓度较高。

而铵离子、硝酸盐和溶解有机碳的浓度较低,科研人员研究了接触混凝土和生物膜后的水样,与仅接触岩体的水样相比,科研人员发现钙、镁和钒的浓度更高,对于其他元素,没有明显的差异。
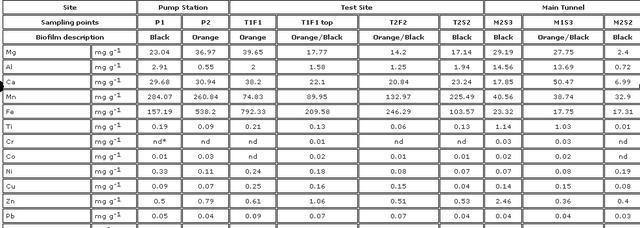
通过对生物膜的化学分析,科研人员发现橙色生物膜中,含有较高浓度的铁和钙,而黑色生物膜中含有较高浓度的锰,科研人员还通过失重,测定确定了生物膜中有机物的含量,结果显示大部分生物膜成分是无机物。

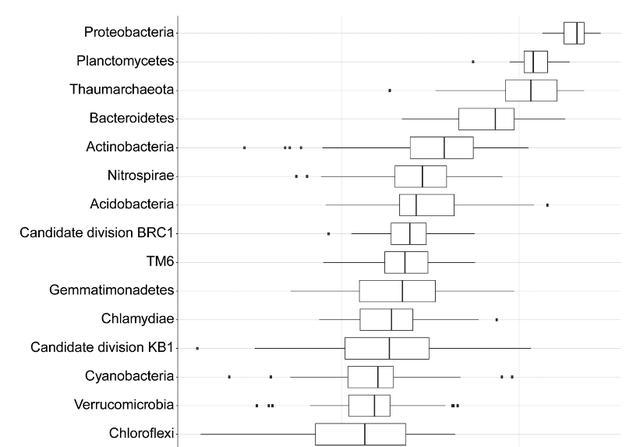
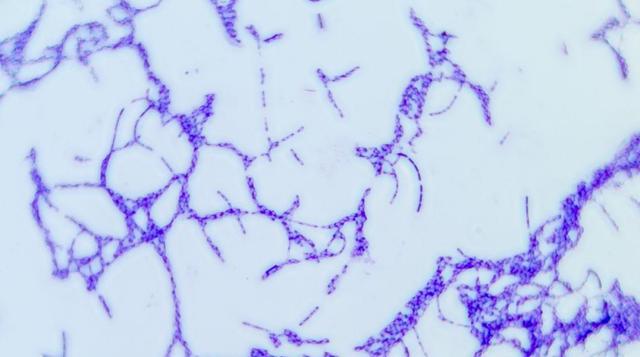
根据16S rRNA SVs的分类分析,科研人员发现变形菌门是生物膜群落的主要成员,占据了群落的44-49%,除了变形菌门,大部分SVs属于隐球菌门、古菌门、拟杆菌门和放线菌门,微酸菌门和硝化螺旋菌门,在64个生物膜样本中的相对序列丰度,超过了总群落的2%。
为了更直观地了解这些结果,科研人员绘制了一个箱线图,展示了生物膜中前15个主要门的情况,阅读量采用对数刻度显示,在箱线图中,粗体垂直线代表中位数,箱体边界代表25%和75%分位数,排除异常值的水平线代表最小值和最大值,而点表示异常值。
这些分析结果表明不同的菌门在生物膜群落中,扮演着重要的角色,并且变形菌门是最主要的成员之一,微酸菌门和硝化螺旋菌门,在样本中的相对序列丰度也相对较高,这些信息有助于科研人员更好地了解生物膜的组成,和生态系统中不同微生物的相对丰度。
海底隧道钢筋喷射混凝土中,蕴藏的微生物群落,对于海底隧道的生物破坏,具有重要意义,通过深入研究和了解这些微生物群落,科研人员可以更好地应对,和解决海底隧道钢筋喷射混凝土的恶化问题,保障隧道的结构完整性和使用安全性。
结语
通过深入研究和了解微生物的特性和作用机制,科研人员可以制定合理有效的预防和控制策略,保障隧道的结构完整性和使用安全性,这需要工程界、学术界和政府部门的共同努力与支持,才能在海底隧道建设和维护中取得更大的成功。
参考文献
1. Albertsen M, Karst SM, Ziegler AS, Kirkegaard RH, Nielsen PH. 2015. Back to basics-the influence of DNA extraction and primer choice on phylogenetic analysis of activated sludge communities. PloS One. 10:e0132783 doi: 10.1371/journal.pone.0132783 [Crossref], [PubMed], [Web of Science (R)], [Google Scholar]
2. Bastidas-Arteaga E, Sánchez-Silva M, Chateauneuf A, Silva MR. 2008. Coupled reliability model of biodeterioration, chloride ingress and cracking for reinforced concrete structures. Struct Saf. 30:110–129. doi: 10.1016/j.strusafe.2006.09.001 [Crossref], [Web of Science (R)], [Google Scholar]
3. Battin TJ, Besemer K, Bengtsson MM, Romani AM, Packmann AI. 2016. The ecology and biogeochemistry of stream biofilms. Nat Rev Microbiol. 14:251–263. doi: 10.1038/nrmicro.2016.15 [Crossref], [PubMed], [Web of Science (R)], [Google Scholar]
4. Beech IB, Sunner J. 2004. Biocorrosion: towards understanding interactions between biofilms and metals. Curr Opin Biotechnol. 15:181–186. doi: 10.1016/j.copbio.2004.05.001 [Crossref], [PubMed], [Web of Science (R)], [Google Scholar]
5. Bertron A. 2014. Understanding interactions between cementitious materials and microorganisms: a key to sustainable and safe concrete structures in various context. Mater Struct. 47:1787–1806. doi: 10.1617/s11527-014-0433-1 [Crossref], [Web of Science (R)], [Google Scholar]















