小黑麦的适应性和潜力:植物胁迫条件下抗氧化酶活性的调控与响应
引言
小黑麦作为一种植物,其适应性和潜力备受关注,在植物生长发育过程中,面临各种胁迫条件是不可避免的。
而植物胁迫条件下,活性氧自由基的产生会造成细胞内氧化应激,并对植物的生理代谢及生长发育产生负面影响,为了应对这种氧化应激,植物通过启动抗氧化系统,来增强自身的抗逆能力,其中抗氧化酶活性起着重要的调控作用。

小黑麦的适应性和潜力
小黑麦是一种人工培育的作物,是将小麦和黑麦进行杂交形成的混合种,总体而言,小黑麦结合了小麦的高产潜力和黑麦对生物和非生物胁迫的耐受性,使其更适合在边缘地区生产。
小黑麦可以作为改良土壤的作物,其广泛的根系可以固定容易受到侵蚀的土壤,并为土壤微生物提供良好的转化为亚土壤有机碳的基质。
尽管小黑麦是一种新的作物,但其生产的好处是巨大的,这也是它被30多个国家广泛采用的原因,而且种植面积还在不断增加。
全球主要的小黑麦生产国包括德国、法国、波兰、澳大利亚、白俄罗斯,根据粮食和农业组织的数据,到2005年,在全球28个国家收获了,1350万吨的小黑麦谷物。
近年来,小黑麦作为一种潜在的能源作物受到了关注,并且目前正在研究该作物,生物质在生物乙醇生产中的利用,人们对小黑麦的兴趣主要集中在,两个潜在的用途领域,即谷物的使用以及作为饲料作物的利用。
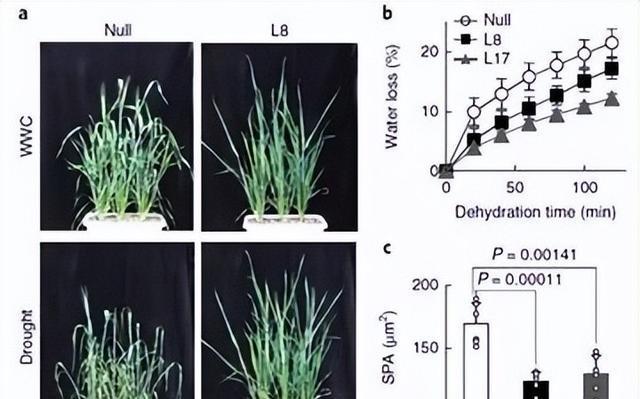
干旱胁迫是影响作物产量的最主要因素,特别是在干旱和半干旱地区的灌溉农业中,这种胁迫会引发植物中各种生化和生理反应,作为一种生存机制。

干旱胁迫直接影响光合作用装置,主要是通过破坏光合作用的各个主要组分,包括类囊体电子传递、碳还原循环和气孔对二氧化碳供应的控制,同时伴随着碳水化合物的积累、脂质过氧化破坏和水分平衡的紊乱。
它打破了活性氧自由基的产生与抗氧化防御系统之间的平衡,导致ROS的积累,从而对蛋白质、膜脂和DNA链的氧化应激和破坏。
在根际土壤中的众多微生物中,有些对植物的生长促进起到积极作用,这些微生物是一些生物肥料,如促生根际细菌,它们定殖于许多植物物种的根际土壤和根部,并对植物产生有益影响。

PGPR促进植物生长的机制尚不完全清楚,但被认为包括以下几个方面:通过生成铁载体产生植物激素来对抗植物病原微生物、无菌固氮、合成抗生素、酶和/或杀真菌化合物,以及溶解矿物磷和其他养分。
利用根际微生物是一种替代策略,可以改善植物在应激环境下的表现,并因此通过不同的机制增强植物生长。
菌根是由植物根与真菌组成的一种共生关系,它们还为植物提供其他好处,包括产生/积累次生代谢物、在渗透胁迫下进行渗透调节、改善固氮、增强光合作用速率以及增加对生物性和非生物性胁迫的抵抗力。
菌根用于增强寄主植物的水分关系的机制尚不十分清楚,然而,这可能是通过增加外生菌丝对水的吸收、调节气孔器官、提高抗氧化酶活性,和吸收养分来实现的。
一项在水分胁迫环境下,进行的小麦研究表明,菌根接种提高了抗坏血酸过氧化物酶,和过氧化氢酶等抗氧化酶的活性,与未接种的对照植物相比,菌根通过改变寄主植物中水分运动的速率,能促进寄主的水分和生理状况。
研究表明,在干旱胁迫条件下,菌根苗比非菌根苗增加了水分吸收,可能是丛枝菌根菌根的菌丝扩大了寄主植物根系的吸收区域,并增强了根部的吸水能力。

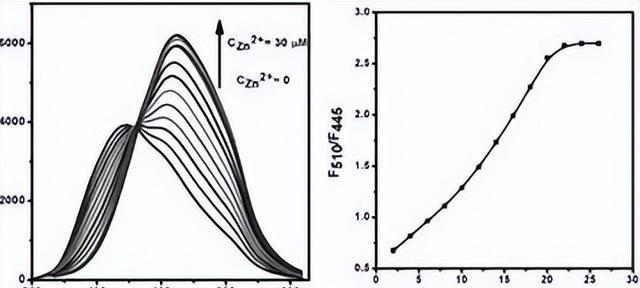
锌是生物系统中的一种必需微量营养素,对酶和蛋白质的生理功能具有至关重要的作用,参与许多生化途径、光合作用、酶系统激活和蛋白质合成,施用锌可以增强苔藓体膜中的光化学反应、PSII的电子传递,并提高光合速率和叶绿素含量。
叶面喷施锌可以增强水稻叶片中的碳酸酐酶活性,从而增加光合作用,碳酸酐酶被认为是一个含锌酶,参与光合作用。类似地,在施用锌处理的茄子苗中,超氧化物歧化酶、过氧化氢酶和抗坏血酸过氧化物酶的活性增加。
干旱是限制植物生长和作物产量的,最严重的非生物胁迫因素,许多植物的生理过程,都会受到干旱胁迫的影响,包括光合作用、酶活性和膜稳定性,全球有10亿公顷的超干旱地区,有54.5亿公顷的干旱、半干旱和亚湿润地区。

世界上70%的干旱土地用于农业,产量有限,作物产量取决于干旱的程度,由于在干旱和半干旱地区,小黑麦的生长期,受到水分限制条件的影响,这会影响抗氧化酶活性、PSII的光合效率、叶绿素含量,和气孔导度等生化和生理反应。
施用生物肥料和锌,是缓解干旱胁迫影响的重要策略之一,生物肥料可以改善非胁迫,和胁迫条件下植物的表现,小黑麦对锌缺乏非常敏感,锌对叶绿素形成、生长激素刺激、碳水化合物合成、酶活性和生殖过程都是必需的。
植物胁迫条件下抗氧化酶活性的影响
当植物遭受各种非生物胁迫时,会产生一些ROS,如超氧阴离子、过氧化氢、羟基自由基和单线态氧,这些ROS可能引发破坏性的氧化过程,如脂质过氧化、叶绿素脱色、蛋白质氧化和核酸损伤。
研究报告称,当植物暴露在水分胁迫下时,抗氧化酶的活性增加,在胁迫环境下改善植物生长可能归因于,酶抗氧化系统在减轻氧化影响方面的显著作用,这一机制通常在小黑麦中得到了指出。
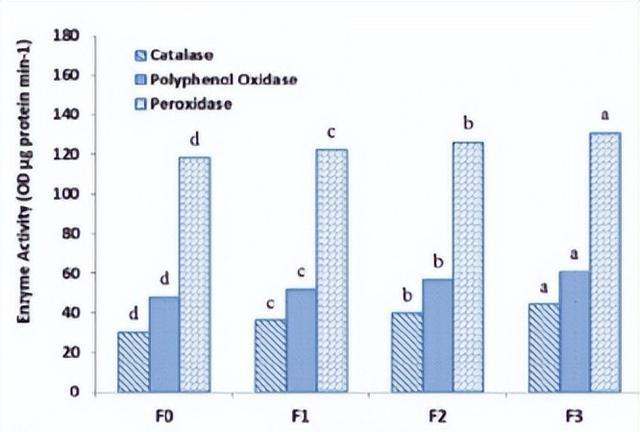
在水分限制下接种PGPR、菌根真菌及二者同时应用显著提高了小黑麦CAT、PPO和POD酶的活性,研究人员的结果显示,与F0相比,在施用生物肥料F3的情况下,CAT、PPO和POD的活性分别增加了约46.4%、27.6%和10.3%。
与Zn0相比,当纳米氧化锌作为Zn3施用时,抗氧化酶的活性增加。因此,与Zn0相比,纳米氧化锌叶面喷施作为Zn3,使CAT、PPO和POD的活性分别增加了约24.4%、25.2%和10.7%,已知锌对生物膜具有稳定和保护作用,可以抵御氧化和过氧化损伤。
自由基的产生和自由基防御之间的平衡决定了系统的存活,锌可能在通过增强植物抗氧化系统来调节自由基及其相关破坏效应方面发挥作用,在研究中,锌的施用增加了抗氧化酶的活性,这表明了锌在缓解胁迫效应方面的影响。
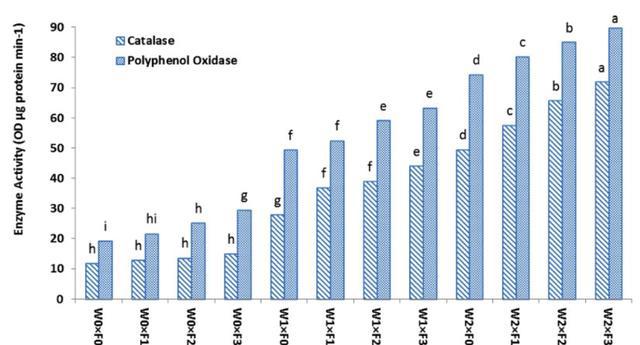
水分限制×生物肥料的效果显示,严重水分限制和生物肥料F3施用时,CAT和PPO的最大活性,W0F0的CAT和PPO的活性最低,另一方面,在最高水分限制和生物肥料水平与相比,CAT和PPO酶的活性增加了约45.1%和20.6%。
水分限制×纳米氧化锌的效应显示,在W2Zn3处理中获得了最高的CAT酶活性,而最低的活性观察到在W0Zn0处理中。与W2Zn0相比,W2Zn3处理中CAT酶活性增加了约18.8%。

CAT、POD和PPO活性的持续增加,表明这些酶在干旱胁迫下是,三个主要的将过氧化氢进行解毒的酶,所有植物物种天然地具有各种防御网络,以防止它们的细胞受到ROS的有害影响,其中包括酶和非酶抗氧化剂。
CAT和POD是细胞中,构成主要H2O2清除系统的两种酶,在胁迫条件下,这些酶的活性会发生变化,而这种变化的程度可能与植物的胁迫耐受性相关。
为评估植物的水分状况,叶片水势和相对含水量,是用来研究植物对干旱胁迫,生理响应的重要参数。

研究人员指出,在大多数植物中,这些参数在水分不足时会下降,植物在干旱胁迫下相对含水量的降低,可能取决于植物活力的减弱,并且已经在许多植物中观察到。
叶片相对含水量的降低,可能与胁迫条件下水分供应不足,或根系无法通过减少吸收表面积,来补偿蒸腾损失的水分有关。
报道指出,菌根根系由于其额外的基质菌丝,可以探索更多的土壤体积,使其比非菌根植物更容易吸收,和转运更多的营养物质,良好的水分状况可能导致根系的活性和导水性增加。

以往的研究发现,与非菌根植物相比,菌根植物通常显示出更高的叶片相对含水量,和水分利用效率,接种PGPR分离物的处理在正常条件下,将相对含水量从5%增加到16%,在胁迫条件下增加了21.7-28.4%,与未接种的对照相比。
锌在维持相对含水量方面的改善作用,可能归因于对导管组织的改善,水限制、生物肥料和纳米氧化锌,对叶绿素含量产生了显著影响。
在开花期、抽穗期和灌浆期,W0F3Zn3处理获得了最高的叶绿素含量,而W2F0Zn0处理获得了最低的叶绿素含量,水限制导致叶绿素含量的降低,而施用生物肥料和纳米氧化锌则增加了这些特性的数值。

结果显示,在严重的水限制条件下,施用生物肥料和叶面喷施纳米氧化锌,使叶绿素含量相较于相同水限制水平下的F0和Zn0,分别增加了23.5%、32.7%和33.3%。
施用生物肥料和纳米氧化锌,增加了叶绿素含量,这表明生物肥料和锌,对缓解胁迫效应具有影响,叶绿素含量下降的主要原因,可能是由ROS引起的降解作用,另一个导致叶绿素下降的原因,是使用谷氨酸前体合成脯氨酸,这是一种逆境应答的代谢产物。
同时,叶绿素含量的减少,被认为是水分胁迫条件下氧化应激和叶绿素降解的典型症状,严重的干旱胁迫还通过影响叶绿素组分,和损害光合器件导致植物光合作用受到抑制。
根据报道,接种了Glomus intraradices菌根真菌的植物,具有较高的叶绿素密度,而未接种菌根真菌的植物则没有,研究表明表明,细菌菌株的接种可以增加莴苣的叶绿素含量,与对照组相比。
锌参与了叶绿素的合成,锌缺乏不仅会导致叶绿素含量大幅下降,还会严重损害叶绿体的微观结构。
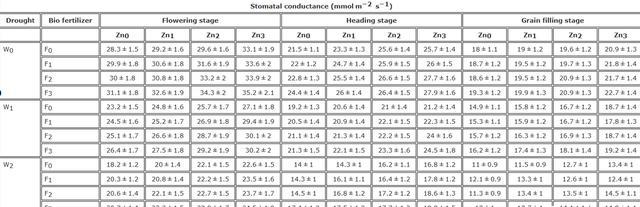
气孔导度测量结果显示,水分限制条件下气孔导度降低。在正常灌溉条件下,施用生物肥料和纳米氧化锌时,最高的气孔导度分别为开花期35.2毫摩尔每平方米每秒、抽穗期27.9毫摩尔每平方米每秒和灌浆期22.7毫摩尔每平方米每秒。

最低气孔导度观察到于W2F0Zn0处理中,研究结果显示,在严重水分限制条件下,与相同水分限制水平下的,不施用生物肥料和纳米氧化锌相比,施用F3和Zn3可分别使开花期气孔导度增加约34.6%,抽穗期增加42.1%,灌浆期增加35.4%。
在水分不足的情况下,大多数植物会关闭气孔,以降低蒸腾速率,进一步限制水分流失到环境中,这个过程由根部产生的信号分子脱落酸介导,气孔闭合是由于叶片弛张,和大气水蒸气压力降低,以及根部产生的化学信号而应对干旱和盐碱胁迫。
通常在应对胁迫条件下,光合速率的降低归因于肾型组织传导,和中度以及严重胁迫下的气孔闭合,干旱条件下的植物为了保留水分,因此气孔导度较低。

许多报告显示,在干旱胁迫的初始阶段,气孔通常会闭合,从而增加了水分利用效率,已知气孔闭合对水分蒸腾的抑制作用,要大于对CO2扩散进叶片组织的作用。
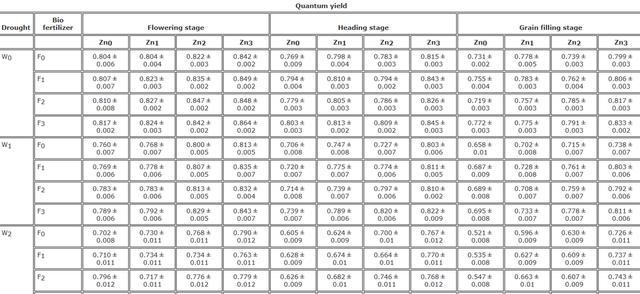
水分限制、生物肥料和纳米氧化锌的应用显著影响了量子产量,在开花、抽穗和灌浆阶段,W0F3Zn3分别获得了最高的量子产量,而W2F0Zn0的量子产量最低。
结果显示,在严重的水分限制下,与F0和Zn0相比,施用生物肥料F3以及纳米氧化锌Zn3可以使开花、抽穗和灌浆阶段的,量子产量分别增加约14.8%、28.7%和43.7%。
叶绿素荧光测量已成为,研究光合作用装置功能,和植物对环境胁迫响应的广泛应用方法,是一种强大的工具,通过叶绿素荧光参数Fv/Fm可以,快速简便地探测环境胁迫,Fv/Fm是PSII初级光化学,最大量子产量的一个非常有用的相对测量指标。
根据研究,光系统II的光化学效率由Fv/Fm比值决定,在干旱胁迫期间显著降低,PSII的损伤会导致叶绿素荧光发生变化,叶绿素荧光已被广泛应用作为一种强大可靠的无创方法,用于评估环境胁迫条件下,光系统II功能的变化和反映初级光合过程。
光系统中存在的光合色素被应力因子损坏,从而降低了两个光系统的吸光效率,进而降低了光合能力,荧光诱导参数及其比值常被用来确定许多受到各种胁迫的物种叶片中的一些代谢紊乱。

根据实验证明,菌根真菌能增加PSII光化学量子产量,尽管植物PSII反应中心被破坏,但在菌根存在的情况下植物的生长增加。AMF共生关系能提高叶绿体对激发能的捕获效率,并增加光适应叶片中PSII的光化学能力。
通常情况下,丛枝菌根真菌,通过改善植物的营养状况,和激活介导基因来提高Fv/Fm,PGPR能通过消除病原微生物、溶解不溶性磷酸盐以及产生植物生长调节剂来改善植物生长。
通过改善植物的营养状况,特别是植物光合作用所需的有效磷元素,以及改善水分胁迫下的光合作用和植物生长,Fv/Fm得以提高。
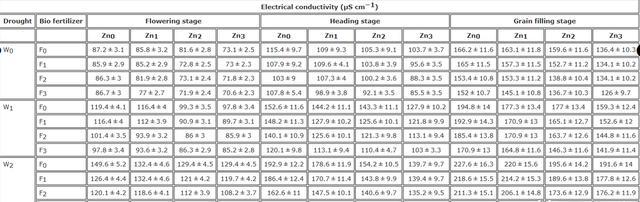
在水限制条件下,电导率显著增加,在水限制条件下,接种PGPR、菌根真菌以及两者的生物肥料均能降低三粒小麦的电导率,施用纳米氧化锌也能显著降低电导率,在开花、抽穗和灌浆期,W2F0Zn0处理的电导率最高。
在开花期、抽穗期和灌浆期,电导率最低的处理分别为W0、F3和Zn3。与W2F0Zn0相比,W2F3Zn3处理的电导率在开花、抽穗和灌浆期分别减少了约28.4%、29.5%和25%。
结果还表明,不同灌溉制度对谷物产量有显著差异,与正常灌溉处理的数据相比,适度和严重的水限制导致谷物产量下降,在正常灌溉和水限制条件下,施用生物肥料和纳米氧化锌可以提高谷物产量。
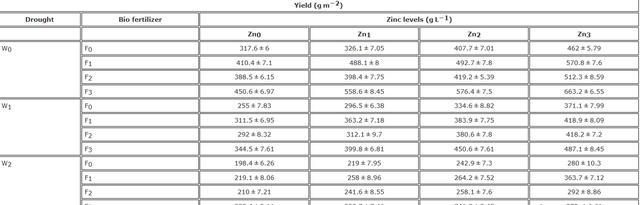
均值比较显示,在正常灌溉条件下施用F3生物肥料和Zn3纳米氧化锌时,谷物产量最高。W2F0Zn0处理获得的产量最低。
研究人员提出了共接种PGPR和AM真菌,作为一种有效的程序来增加产量和植物生长,许多研究者指出,生物肥料可以减轻干旱胁迫,对植物生长的不利影响,据报道,接种PGPR可以显著增加重要农作物的生长和产量。
据报道,叶面施用锌可以显著增加其他作物的谷物产量,研究结果表明,水限制降低了植物的产量、光量子产量、气孔导度、叶绿素含量和相对水分含量,但CAT、POD和PPO酶的活性及电导率增加。

在水限制条件下施用生物肥料和纳米氧化锌可以增加谷物产量、叶绿素含量、抗氧化酶的活性、光量子产量、气孔导度和相对水分含量,而电导率降低。
这表明植物通过合成抗氧化酶,和降低气孔导度等防御机制,来改善应对压力的效果,并且建议在水限制条件下,使用生物肥料和纳米氧化锌,以提高小黑麦的产量。
结语
研究表明,小黑麦在面对植物胁迫条件时,能够调节抗氧化酶的活性来应对活性氧自由基的损害,这揭示了小黑麦植物在适应恶劣环境方面的潜力。

进一步研究小黑麦适应性和潜力的机制,有助于揭示植物逆境适应性的基本原理,为农业生产和生态环境保护提供理论指导和实践支持,因此,关注小黑麦的适应性和潜力以及其与植物胁迫条件下抗氧化酶活性的关联,对于推动农业可持续发展具有重要意义。
参考文献
1.Ahmad F, Ahmad I, Khan MS. 2006. Screening of free-living rhizospheric bacteria for their multiple plant growth promoting activities. Microbiol Res. 136:173–181. [Google Scholar]
2.Ahmad P, Prasad MNV. 2012. Abiotic stress responses in plants: metabolism, productivity and sustainability. New York: Springer. [Crossref], [Google Scholar]
3.Allen DJ, Ort DR. 2001. Impacts of chilling temperatures on photosynthesis in warm-climate plants. Trends Plant Sci. 6:36–42.
4.Arnon DI. 1949. Copper enzymes in isolated chloroplast polyphenol oxidase in Beta vulgaris. Plant Physiol. 24:1–15. doi: 10.1104/pp.24.1.1
5.Auge RM, Schekel KA, Wample RL. 1986. Osmotic adjustment in leaves of VA mycorrhizal and nonmycorrhizal rose plants in response to drought stress. Plant Physiol. 82:670–765. doi: 10.1104/pp.82.3.765















